Esta unidad constituye un pilar fundamental en la atención prehospitalaria, pues casi el 100% de las patologías que enfrentamos en urgencias pueden derivar de diversas maneras en alguno de los tipos de shock.
El shock es una condición caracterizada por una reducción profunda y generalizada del aporte efectivo de oxígeno a los tejidos, inicialmente es reversible, pero se torna irreversible pudiendo llegar a la disfunción multiorgánica y a la muerte.
La condición de shock puede ocurrir por causa de un contenido sanguíneo insuficiente, en este caso es llamado hipovolémico, que puede ser hemorrágico o no hemorrágico. Es decir, la pérdida puede ser directa de volumen sanguíneo o indirecta por vía digestiva, en forma de vómitos o diarrea, renal, como orina, o cutánea, en forma de sudor. Otra forma de llegar al estado de shock, es la falla de la función cardíaca de bomba, esto puede ocurrir por causa extra cardíaca, por obstrucción al flujo de eyección, al retorno venoso o a la contracción cardíaca, en este caso es llamado shock obstructivo. Existen tres causas principales de shock obstructivo, que serán detalladas más adelante, estas son; el neumotórax a tensión, la tromboembolia pulmonar y el taponamiento cardíaco.
La bomba cardíaca también puede fallar por causas intrínsecas. Esto puede ocurrir por enfermedades miocárdicas, en las que ocurre una disminución de la fuerza de contracción muscular, y de la fracción de eyección sanguínea, o por alteración de la frecuencia cardíaca, en este caso puede ocurrir taquicardia o bradicardia, en todos estos casos el gasto cardíaco se verá afectado.
Otra alteración que puede llevar a la condición de shock, es la alteración del continente, es decir del diámetro de los vasos sanguíneos. En este caso es llamado shock distributivo, ya que ocurre vasodilatación periférica y vasoconstricción central en venas y arterias, lo que distribuye de manera anómala la sangre en condición de stress, esto es llamado shock distributivo. Las principales causas de shock distributivo son; infecciones, en el caso del shock séptico, alergias, en el caso del shock anafiláctico, y daño en la médula espinal, en el caso del shock neurogénico.

Es muy raro encontrar personas que solo sufran de un tipo de shock, es por eso que se habla del shock combinado, en el que la falla predominante puede ser la bomba, el contenido o el continente, pero pueden existir otros tipos de shock subyacentes. Por ejemplo, durante el shock séptico ocurre vasodilatación periférica con aumento de la permeabilidad vascular, lo que favorece la pérdida de volumen sanguíneo, en este caso es un shock combinado predominantemente por falla del continente, pero con un componente hipovolémico subyacente.
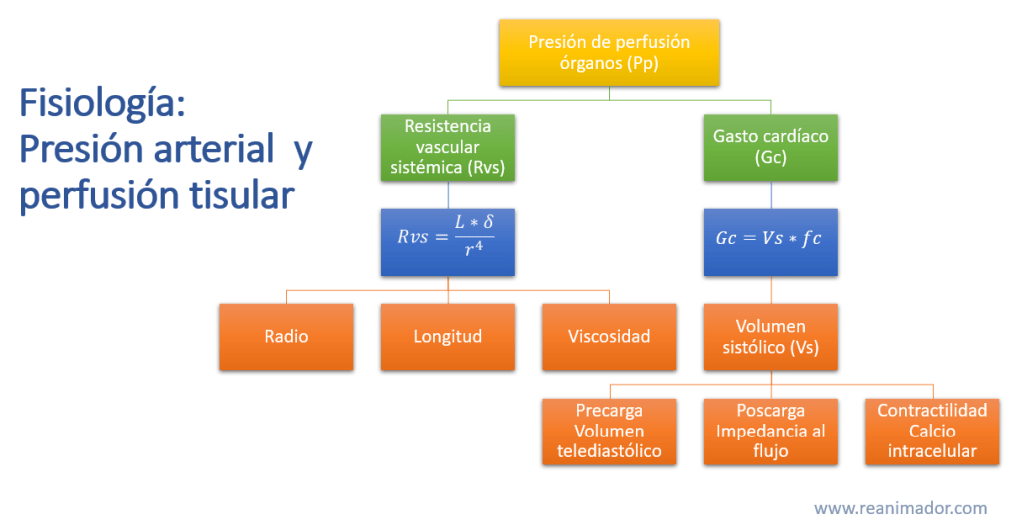
Para mantener la perfusión de los tejidos, cada órgano posee características especiales, sin embargo, el sistema vascular posee dos mecanismos generales que permiten mantener la presión de perfusión del organismo en su conjunto, estos son, la resistencia vascular sistémica y el gasto cardíaco. La resistencia vascular sistémica es directamente proporcional al largo del sistema vascular y la viscosidad de la sangre, e inversamente proporcional al radio de los vasos sanguíneos elevado a la cuarta potencia. La longitud de los vasos sanguíneos y la viscosidad permanecen constantes, por lo tanto el radio arterial es el determinante principal de la resistencia vascular sistémica. El gasto cardíaco es directamente proporcional al volumen sistólico y la frecuencia cardíaca, mientras que el volumen sistólico es modificado por la precarga, representada por el volumen ventricular al final de la diástole, la poscarga, que se define como la impedancia al flujo sanguíneo, y la fuerza de contracción miocárdica, dependiente de la disponibilidad de calcio intracelular. Los principales mecanismos de control de la precarga y poscarga son la alteración del retorno venoso, en el caso de la precarga, mientras que para el control de la poscarga el sistema modifica la resistencia vascular, a través del radio de los vasos sanguíneos.
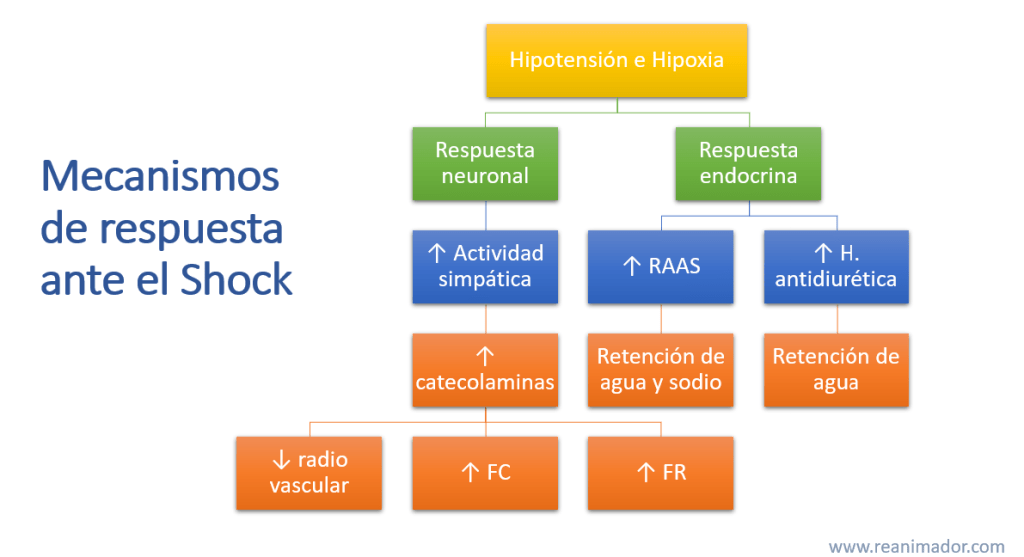
Cuando el shock se encuentra instalado ocurre hipotensión e hipoxia, en este caso el organismo utiliza sus mecanismos de respuesta. El primero es la respuesta neuronal, cuyo principal mediador es el sistema nervioso simpático, que estimula la secreción suprarrenal de catecolaminas, principalmente adrenalina y noradrenalina, las cuales disminuyen el radio vascular periférico, aumentan la frecuencia cardíaca, la frecuencia respiratoria y el radio vascular de los órganos nobles, logrando un aumento en el gasto cardíaco y redistribuyendo la perfusión inicialmente al corazón, cerebro, pulmones, riñones e hígado, para luego avanzado el shock, privilegiar solo cerebro, corazón y pulmones. El segundo mecanismo de respuesta sistémica es endocrina, en este nivel ocurre un aumento de la actividad del sistema renina angiotensina aldosterona, lo que logra retener sodio y agua a nivel renal, y de la hormona antidiurética, que logra la retención de agua. En suma, ambos mecanismos de respuesta buscan aumentar el gasto cardíaco, a través del aumento de la resistencia vascular periférica, de la frecuencia cardíaca y del volumen sistólico, aumentando la precarga y la poscarga cardíaca.
Los mecanismos de respuesta buscan mantener la perfusión tisular, sin embargo cuando estos mecanismos fallan ocurren alteraciones en distinto nivel que explican la fisiopatología del shock. A nivel celular la respuesta depende del umbral anaeróbico del tejido, sin embargo, antes o después, ocurre déficit de ATP, acidosis metabólica, incremento de los niveles de sodio intracelular, lo que lleva a edema, destrucción de cromosomas, producción de radicales libres, y muerte celular (apoptosis) por aumento de la actividad anaeróbica, ante la falta de oxígeno. Inicialmente todo este material de desecho genera solo daño local, gracias a la contracción arteriolar, sin embargo cuando el shock avanza, ocurre vaso dilatación arteriolar esparciendo el daño al resto del cuerpo. Como se dijo anteriormente, una de las respuestas es aumentar la frecuencia respiratoria, lo que lleva a una alcalosis respiratoria transitoria por disminución de los niveles de dióxido de carbono. Esta respuesta requiere un gran consumo de ATP, por lo tanto cuando las reservas de ATP disminuyen la frecuencia respiratoria baja, esto induce una acidosis respiratoria que empeora la acidosis metabólica antes mencionada. La permeabilidad vascular se encuentra aumentada a nivel sistémico, lo que en términos pulmonares se traduce en traspaso de plasma sanguíneo desde el intravascular al espacio alveolar, lo que finaliza en síndrome de distrés respiratorio agudo, patología que puede terminar con la vida del paciente. Finalmente la acidosis generalizada, la hipoxia y la hipoperfusión generan encefalopatía hipóxica, con lo que el paciente sufre compromiso de conciencia y, eventualmente, la muerte.
La fisiopatología antes descrita es común a todos los shock, sin embargo existen algunas diferencias respecto al tipo de shock, que son importantes de señalar, porque podrían determinar diferencias terapéuticas. En el caso de los shock hipovolémico, cardiogénico y obstructivo, ocurre el aumento de la resistencia vascular sistémica con disminución del gasto cardíaco, en cambio en los shock de tipo distributivos la resistencia vascular sistémica se ve disminuida. Estas diferencias podrían marcar cambios en la conducta terapéutica respecto del uso de fármacos vasopresores.
Como ya se ha mencionado, el shock se presenta en distintos estados evolutivos, avanza desde fase compensada, hasta una irreversible, pasando por una fase descompensada. La fase compensada se caracteriza por taquicardia y vaso constricción, que son capaces de sostener la presión arterial, que es normal en esta etapa. La vasoconstricción explica el resto de la sintomatología a este nivel, dentro de la que se encuentra, manos y pies fríos, mucosas pálidas y llene capilar lento. Durante el shock descompensados la frecuencia cardíaca y la vasoconstricción, no son capaces de sostener la presión arterial, por lo tanto el paciente se encuentra hipotenso, pálido, diaforético y su frecuencia cardíaca supera los 120 latidos por minuto y la respiratoria supera las30 respiraciones por minuto, en esta etapa el sistema vascular le resta prioridad a la perfusión renal, por lo que el paciente deja de orinar. Finalmente en una fase Irreversible aparece hipotensión profunda, bradicardia, bradipnea y compromiso de conciencia, todos estos signos y síntomas son fruto de un alto nivel de fatiga y acidosis, la que finalmente lleva al paciente a la muerte de no ser revertido el cuadro en etapas previas.

1.1 Evaluación prehospitalaria del paciente en Shock
Para la evaluación del paciente en shock en el ámbito prehospitalario usaremos la misma herramienta que en todos los demás pacientes, la evaluación sistemática.
La evaluación sistemática indica que lo primero que haremos al evaluar a un paciente en shock es obtener una impresión inicial de la seguridad y la información que nos entregue la escena y el paciente. Cuando confirme que la escena es segura observe si el paciente parece consciente o inconsciente. Si el paciente parece consciente realice una evaluación primaria usando la herramienta xABCDE, y una anamnesis usando SAMPLER y O P Q R S T. En cambio, si el paciente se encuentra inconsciente verifique pulso, respiración y respuesta, si presenta alguna de las anteriores vuelva a la evaluación primaria, si no realice maniobras de soporte vital básico o avanzado, según sea su nivel de experiencia.
Para jerarquizar la gravedad y priorizar la atención de cualquier paciente en el ambiente prehospitalario usaremos la herramienta xABCDE. Donde la x hace referencia a la presencia de hemorragias exanguinantes, estas deben ser contenidas de inmediato. La letra A se refiere a la permeabilidad de la vía aérea, el indicador de permeabilidad es el ruido, cuando la respiración es ruidosa los reanimadores deben realizar maniobras para permeabilizar la vía aérea, por ejemplo, maniobra frente mentón, tracción mandibular, aspiración de secreciones o usar una cánula orofaríngea. La letra B hace referencia a la vía aérea, donde su mayor preocupación debe ser la frecuencia respiratoria y la saturación parcial de oxígeno, aunque no debe descuidar el resto de los factores que afectan la ventilación, como la simetría del tórax, el uso de musculatura accesoria o el patrón ventilatorio. En la letra C encontrará la mayor parte de las alteraciones ligadas al shock, en este punto debe evaluar la frecuencia cardíaca, la presión arterial el llene capilar, el estado de la piel y las venas yugulares en el cuello. La letra D se relaciona con el déficit neurológico, en la que debe enfatizar en el estado de conciencia del paciente, para esto use inicialmente la escala de AVDI, luego, compleméntela con la escala de coma de Glasgow, para luego continuar con otras evaluaciones como la glicemia, pupilas o la escala de ACV de Cincinnati. Finalmente exponga el cuerpo del paciente en busca de otros datos.
Cuando descarte que su paciente no está en riesgo vital inminente inicie una anamnesis guiándose por la herramienta SAMPLE, donde la S significa signos y síntomas, los signos y síntomas en el Shock son muy diferentes según su forma de presentación, en este capítulo encontrará información detallada de cada uno de ellos. Cuando pesquise los signos o síntomas, utilice la nemotecnia O P Q R S T para indagar acerca de ellos, para eso considere que la O, significa inicio, por onset en inglés, en la P averigüe las formas de presentación del síntoma, en la Q las características del síntoma, en la R si el dolor se irradia en alguna dirección, en la S la severidad y en la T el tiempo de evolución del signo o del síntoma. Continuando con la evaluación SAMPLE pregunte respecto a alergias, medicamentos, historia previa, la última comida y las características del evento. Para más detalles de evaluación sistemática revise el capítulo referente a evaluación de pacientes en el ambiente prehospitalario.
1.1.1 Shock hipovolémico
El shock hipovolémico se define como la incapacidad vascular de transportar oxígeno a los tejidos producto de una precarga disminuida por pérdida de volumen intravascular. Tras lo cual, el organismo compensa aumentando la resistencia vascular sistémica.
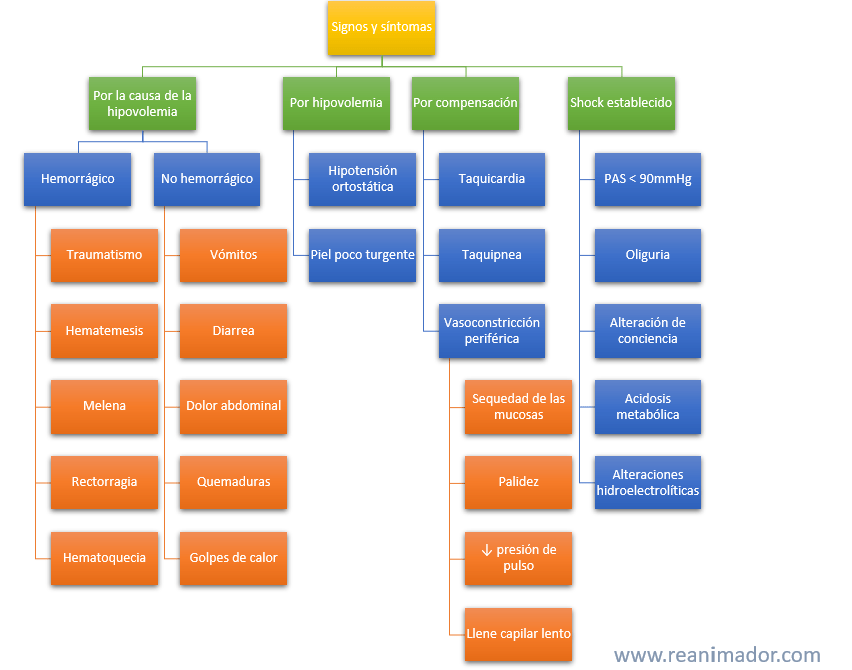
Los signos y síntomas del shock hipovolémico son dinámicos, ellos pueden ser explicados por el estado compensatorio del shock o por las causas de este. Según la causa de la hipovolemia los signos y síntomas serán distintos. Cuando es hemorrágico, la pérdida de sangre puede ser evidente al haber un traumatismo visible, o puede sospecharse cuando afecta órganos internos. De estos, un sistema que habitualmente se ve afectado por hemorragias es el gastrointestinal, cuando esto ocurre el paciente presenta, hematemesis, que es la presencia de sangre en los vómitos, melena, que se define como heces negras y fétidas debido a la presencia de sangre digerida en ellas, rectorragia, que es la pérdida de sangre no digerida proveniente del recto, o hematoquecia, que es la presencia de sangre no digerida en las heces. Otros signos y síntomas asociados a hipovolemia no hemorrágica son vómitos, diarrea y dolor abdominal, pérdida de volumen por quemaduras o en forma de sudor, por ejemplo, cuando el paciente es sometido a golpes de calor. La hipovolemia explica la aparición de hipotensión ortostática y la pérdida de turgencia de la piel, mientras que la compensación a este fenómeno se evidencia por taquicardia, taquipnea y vasoconstricción periférica, cuando este último mecanismo compensatorio aparece, es fácil observarlo en el paciente, pues se manifiesta como sequedad de las mucosas, palidez, disminución de la presión de pulso y llene capilar mayor a 2 segundos. Cuando los mecanismos compensatorios fallan aparecen varios signos clínicos que permiten notar esta situación, en este caso el paciente se mostrará hipotenso, oligúrico, es decir con disminución de la producción de orina y comprometido de conciencia, esto último por hipoxia, acidosis y alteración en la concentración de iones plasmáticos.
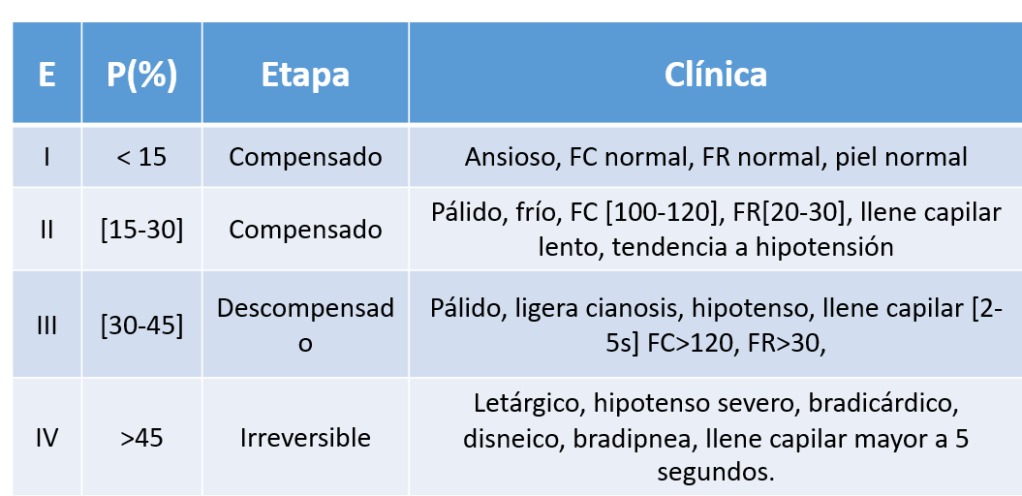
Otra forma de explicar los signos clínicos del paciente es a través de los estados del shock hipovolémico. Cuando se encuentra en estadio 1 ha perdido menos de un 15% del volumen sanguíneo, en este caso el paciente presentará una clínica asociada a una compensación inicial, usted observará una persona ansiosa, pero con constantes vitales dentro de rango normal. En estadio 2, la pérdida de sangre es entre el 15 y el 30%, esos niveles de hipovolemia son compensables por el organismo, por lo que el paciente se verá pálido y frío, además se encontrará taquicárdico hasta 120 latidos por minuto, taquipneico hasta 30 respiraciones por minuto, el llene capilar será lento, y su presión arterial tenderá a la hipotensión. Cuando el shock no es capaz de ser compensado se categoriza como en etapa 3, esto ocurre con pérdidas entre el 30 y 45% del volumen sanguíneo, en este caso observará a una persona pálida, cianótica, hipotensa, taquicárdico con frecuencia cardíaca mayor a 120 latidos por minuto y respiratoria sobre 30 por minuto. Finalmente cuando el paciente pierde más del 45% de su volumen sanguíneo, entra en una fase irreversible, por lo que su presentación clínica será mucho más marcada, presentándose letárgico, en ocasiones inconsciente, y con hipotensión severa y bradicardia.
1.1.2 Shock distributivo
El shock distributivo se define como vasodilatación repentina con aumento de la capacidad vascular y fugas de sangre al tercer espacio en el contexto de sepsis, anafilaxia o pérdida de control de la musculatura vascular. Según su etiología puede clasificarse en, séptico, anafiláctico o neurogénico.
1.1.3 Shock séptico
El Shock séptico es resultado de una respuesta inflamatoria sistémica masiva producto de una infección por cualquier causa.
Cuando los patógenos se instalan en una persona y la infectan ocurren varios fenómenos encadenados. El primero de ellos es el síndrome de respuesta inflamatoria sistémica, que puede ser reconocido cuando la persona presenta 2 o más de los siguientes síntomas; temperatura mayor a 38 o menor a 36 grados Celsius, frecuencia cardíaca mayor a 90 latidos por minuto, frecuencia respiratoria mayor a 20 respiraciones por minuto o recuento de glóbulos blancos mayor a 12.000 por milímetro cúbico. Cuando el síndrome de respuesta inflamatoria sistémica se acompaña de daño de uno más de los siguientes sistemas; respiratorio, renal, hepático, cardiovascular o neurológico, es llamado sepsis grave. Finalmente, cuando la sepsis grave se acompaña de falla cardiovascular, que no responde a tratamiento, es llamado shock séptico
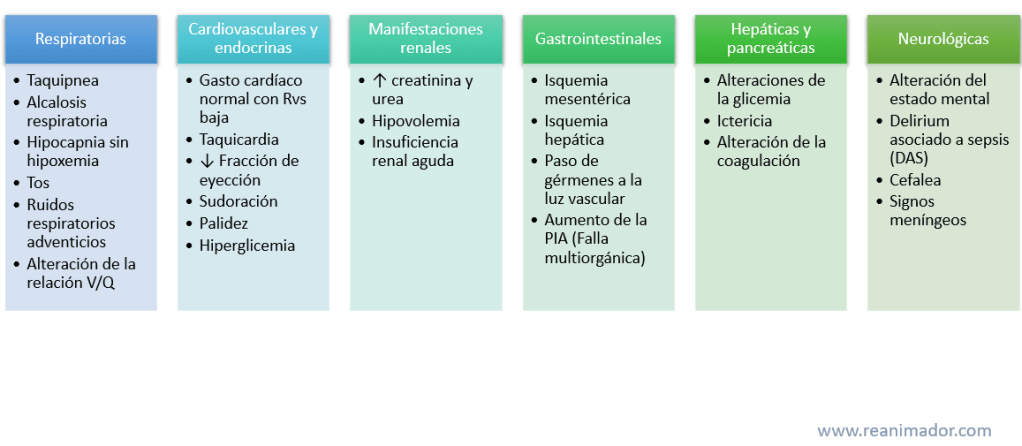
Las manifestaciones clínicas del shock séptico dependen del órgano que se encuentre infectado, cuando es el sistema respiratorio el paciente presentará; taquipnea, alcalosis respiratoria, hipocapnia sin hipoxemia, tos y ruidos respiratorios adventicios. Cuando la infección afecta al sistema cardiovascular las manifestaciones clínicas serán; vasodilatación periférica, la que fisiológicamente, se evidencia con una resistencia vascular sistémica disminuida, con gasto cardíaco normal. Clínicamente el paciente se observará sudoroso, caliente y rojo inicialmente, para luego dar paso a palidez y piel fría. Las manifestaciones renales se relacionan con una insuficiencia renal aguda, que se evidencia con oliguria. Desde el punto de vista gastrointestinal el shock séptico puede mostrar síntomas propios de la patología subyacente, como vómitos o diarrea, así como también, puede mostrar síntomas asociados a la pérdida de irrigación gastrointestinal, apareciendo isquemia mesentérica o hepática, lo que se traduce en el paso de gérmenes desde el sistema gastrointestinal al torrente sanguíneo. A nivel pancreático y hepático el shock puede manifestarse con hiperglicemia e ictericia, que es un color amarillo anaranjado, como manifestación del incremento de bilirrubina. La patología neurológica se mostrará con compromiso de conciencia, delirio, con signos de irritación meníngea, como rigidez de nuca y cefalea. Además de las alteraciones en la coagulación propias de la sepsis del hígado o su hipoperfusión, cuando el shock pasa a fase irreversible el detritus esparcido por el organismo genera un fenómeno llamado coagulación intravascular diseminada, que produce zonas con coagulación aumentada en algunos puntos y disminuida en otros, por lo que el paciente es susceptible a sufrir enfermedades trombóticas o hemorragias indistintamente.
Como se aprecia en el párrafo anterior la sintomatología asociada al shock es muy variada, por eso se han creado múltiples escalas y test que simplifican el diagnóstico, una de esas es la escala de Robson, esta es una abreviación de la escala de evaluación secuencial de falla orgánica (SOFA, por sus siglas en ingles), por lo que también es llamada Q SOFA. Esta indica que existe un alta probabilidad de sepsis grave con dos o más de los siguientes signos; frecuencia respiratoria mayor a 20 por minuto, frecuencia cardíaca mayor a 90 por minuto, presión arterial sistólica menor a 110 milímetros de mercurio, alteración del estado de conciencia, temperatura mayor a 38,3, o glucosa capilar mayor a 119 milígramos por decilitro de sangre. Esta escala no es capaz de discriminar el órgano infectado.

1.1.4 Shock anafiláctico
El shock anafiláctico es la pérdida de perfusión y aporte de oxígeno tisular, producto de una respuesta a hipersensibilidad antígeno anticuerpo, en términos simples es producto de una reacción alérgica severa.
En el 80% de los casos es posible determinar el agente causal de la respuesta antígeno anticuerpo exagerada. Los desencadenantes más comunes de anafilaxia severa en adultos, son las picaduras de insectos o animales, como abejas, medusas, hormigas o avispas. En niños las reacciones alérgicas más severas son producto del consumo de alimentos, dentro de estos los frutos secos y alimentos del mar son los más comunes. Los aditivos de los alimentos procesados también pueden generar reacciones alérgicas. Muchos medios de contraste poseen yodo, por lo que algunos exámenes de imágenes pueden ocasionar reacciones anafilácticas severas. Existen agentes ambientales, como el pelo de animales o el polen, así como algunos materiales clínicos, como el látex, pueden generar reacciones alérgicas severas, respecto al látex es importante señalar que buena parte de los guantes clínicos poseen este material. Otros agentes capaces de desencadenar alergias son los fármacos, por esto siempre antes de administrar un fármaco consulte dirigidamente esta condición. En un 20% de los casos no es posible determinar el agente alergénico.
La exposición a los agentes alérgicos desencadena una serie de procesos patogénicos en aquellas personas hiperreactivas. La reacción inicial es a nivel bioquímico, a través de la liberación de histamina, eosinófilos, heparina y leucotrienos al torrente sanguíneo. Esto produce vasodilatación y aumento de la permeabilidad vascular, broncoconstricción, hipersecreción bronquial y constricción coronaria. Esto se refleja clínicamente en hipotensión por falla de continente y contenido, y dificultad respiratoria.

La muerte por anafilaxia ocurre en el 41% de los casos por shock y en el 31% por asfixia, mientras que en el 9% no se logra determinar la causa. Más del 80% de las muertes ocurre en pacientes asmáticos mal controlados y alérgicos a los frutos secos.
Para realizar el diagnóstico es necesario considerar la aparición aguda de síntomas en dos o más sistemas tras la exposición al agente alergénico. Los signos y síntomas que parecen en la piel y las mucosas son habitualmente evidentes a simple vista, dentro de estos encontramos, edema, Rush cutáneo, que se muestra como un enrojecimiento general de la piel, prurito y urticaria, el paciente relatará que siente picazón o usted lo observará rascando su piel. Desde el punto de vista respiratorio usted observará; disnea, retracciones, cianosis, estridor y sibilancias. A nivel vascular, inicialmente aparecerá taquicardia, para luego dar paso a la hipotensión y el compromiso de conciencia, que son indicadores importantes de shock descompensado. Otro sistema que puede ser afectado es el gastrointestinal, principalmente cuando el alérgeno es consumido vía oral.
La evaluación prehospitalaria del paciente en shock anafiláctico sigue las mismas directrices de la evaluación sistemática, sin embargo, aquí toma especial importancia la A de alergias en la herramienta SAMPLE. Cuando el paciente informa respecto a la presencia de alergias y la clínica es compatible con shock anafiláctico, el resto de la evaluación debe enfocarse en la búsqueda del posible alérgeno, para eso la M de medicamentos debe consultar respecto al uso de antialérgicos y dosis de adrenalina de emergencia, que algunos pacientes con anafilaxia severa tienen siempre a disposición, en la L de última comida puede encontrar la causa de la reacción alérgica, finalmente en la E de evento, es importante recabar información respecto a exposición a alérgenos, cuánto tiempo y hace cuanto estuvo expuesto.
1.1.5 Shock neurogénico
Otra forma de shock distributivo es el neurogénico. En este caso la hipoperfusión es resultado de la pérdida de tono vascular simpático, ocasionado por lesiones graves del sistema nervioso, especialmente de la médula espinal.
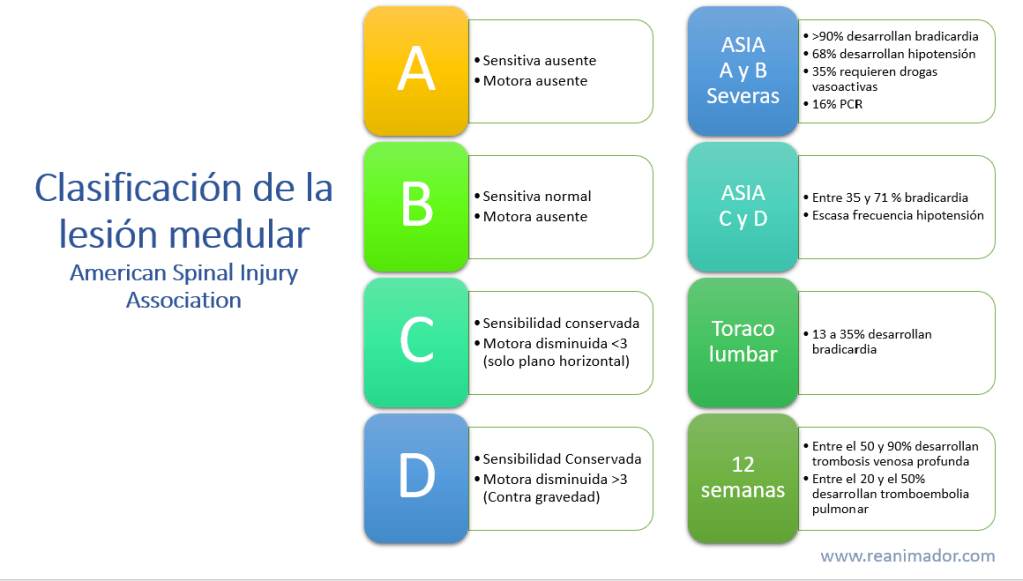
La principal causa de shock neurogénico es la lesión de la médula espinal. Como la médula espinal cumple múltiples funciones, su lesión origina diversa sintomatología según el área dañada, por eso, la Sociedad Americana de Lesión Espinal la clasifica como; ASIA A, en este nivel de lesión el paciente presenta una sección completa de la médula espinal, por eso el paciente no presenta actividad motora ni sensitiva. En la clasificación ASIA B el paciente presenta actividad sensitiva normal, pero motora ausente. La categorización ASIA C indica que el paciente presenta actividad sensitiva conservada y motora disminuida, no es capaz de mover sus extremidades contra la gravedad. Finalmente la jerarquización ASIA D indica que el paciente presenta sensibilidad conservada y fuerza disminuida, pero el paciente es capaz de movilizar sus extremidades contra la gravedad. Esta clasificación es útil para suponer las complicaciones potenciales que pueda presentar el paciente durante su atención, así lesiones ASIA A y B son catalogadas como severas y más del 90% desarrollan bradicardia, el 68% presentan hipotensión, el 33% requieren drogas vasoactivas y el 16% caen en paro cardiorrespiratorio. En cambio pacientes leves y moderados, ASIA C y D desarrollan bradicardia entre un 35 y 71% y rara vez evolucionan con hipotensión. Las alteraciones producto de una lesión medular pueden manifestarse tardíamente, no obstante eso, pueden llegar a ser igual o más graves, por ejemplo, entre el 50 y el 90% desarrollan trombosis venosa profunda, y entre el 20 y 50% desarrollan tromboembolia pulmonar. Estos indicadores empeoran cuando el paciente no recibe medidas preventivas contra la trombosis venosa profunda, como el uso de medias antiembólicas.
Cuando una persona sufre un trauma medular ocurren una serie de procesos en respuesta o a consecuencia del daño. Inicialmente ocurre vasoconstricción y aumento de la contractilidad cardíaca, lo que deriva en un aumento de la presión arterial como consecuencia de la liberación de catecolaminas en respuesta al trauma. Posteriormente ocurre pérdida del control vascular por parte del sistema nervioso simpático, lo que se traduce en hipotensión arterial y shock neurogénico descompensado.
La noxa inicial y la patogenia del trauma medular explican sus manifestaciones clínicas. La pérdida de la fuerza muscular es la alteración más común en el trauma raquimedular, otros signos y síntomas presentes son; alteración de la sensibilidad, hipotensión y taquicardia. Durante las primeras semanas tras el accidente existe un alto riesgo de sufrir arritmias cardíacas, estas pueden ocurrir por pérdida de control simpático con el sistema parasimpático conservado, lo que explica la prevalencia de bradicardia sobre taquicardia. Otro signo clínico importante es la alteración del tono muscular, dentro de los primeros días el paciente presentará hiporreflexia, al pasar el tiempo el tono muscular evoluciona a hiperreflexia. Además de lo anterior, la falta de movilidad, las alteraciones del tono vascular y las alteraciones de la coagulación producto de la hipoperfusión hepática, vuelven al paciente susceptible a sufrir trombosis venosa profunda, con el consiguiente aumento de riesgo de sufrir enfermedades tromboembólicas.
1.1.6 Shock cardiogénico
Cuando el sistema cardiovascular no es capaz de llevar oxígeno a los tejidos a causa de una alteración en la bomba cardíaca, en presencia de un volumen intravascular normal, es llamado shock cardiogénico.
Sin duda, la principal causa de shock cardiogénico es el infarto agudo al miocardio, esto ocurre en el 80% de los pacientes con este tipo de shock. Otras causas posibles son las complicaciones mecánicas. Dentro de las complicaciones mecánicas más comunes se encuentra la insuficiencia de la válvula mitral, la rotura de los músculos papilares y de los ventrículos o el septum interventricular.
Como el shock cardiogénico, al igual que todos los otros tipos de shock, constituyen una enfermedad sistémica, presentan signos generales y por sistema. Los signos generales son hipotensión, definida como una presión sistólica inferior a 90 mmHg o una caída del 30% respecto a su presión arterial basal. La hipoperfusión periférica, es otro factor común que marca la sintomatología del paciente, cuando esto ocurre el paciente se verá pálido, cianótico, frío y con su estado de conciencia comprometido. La insuficiencia cardíaca, origen del shock cardiogénico, puede afectar al ventrículo izquierdo o derecho. Cuando afecta al ventrículo izquierdo, la sangre no será extraída eficientemente desde las venas pulmonares, por lo que el paciente evolucionará disneico, taquipneico, con ruidos agregados a la respiración, cuando estos no estén presentes sospeche de hipovolemia y sin ingurgitación venosa yugular, en la mayoría de los casos. Cuando la insuficiencia cardíaca es derecha, la sangre no será correctamente extraída de las venas cavas, por lo que la sintomatología será sistémica, en la mayoría de los casos no presenta ruidos pulmonares y en el cuello observará ingurgitación venosa yugular. Otros signos y síntomas se presentarán dependiendo del órgano afectado, cuando se afectan los riñones aparecerá oliguria, en este caso de no ser corregido oportunamente el shock el paciente puede sufrir daño renal crónico y requerir hemodiálisis de por vida. Cuando los pulmones se encuentran afectados, sobre todo cuando el paciente presenta insuficiencia cardíaca congestiva izquierda, se verá afectado el intercambio gaseoso, la relación ventilación perfusión y ocurrirá pérdida de surfactante pulmonar, lo que se traducirá en hipoxemia, retracciones, disnea y cianosis. Cuando el daño ocurre a nivel hepático el paciente se torna susceptible a hemorragias y trombosis, debido a alteraciones de la coagulación.
Cuando el paciente entra en estado de shock el sistema cardiovascular intenta compensar de diversas formas, sin embargo esos mecanismos compensatorios no están libres de complicaciones. Como se describe más arriba en este capítulo, un objetivo compensatorio importante es el aumento de la resistencia vascular sistémica, que cuando es efectiva, logra un aumento considerable de la presión arterial, sin embargo, este mecanismo compensatorio genera algunas complicaciones, como el aumento del consumo de oxígeno, y por consiguiente, del metabolismo anaeróbico, lo que produce acidosis láctica e hipoperfusión distal. Otro mecanismo compensatorio es la venodilatación, lo que aumenta la precarga por mayor retorno venoso, esto eventualmente, ante un mal funcionamiento ventricular, podría producir congestión pulmonar.
1.1.7 Shock obstructivo
Cuando la imposibilidad de transportar oxígeno a los tejidos es producto de una falla de bomba de causa extrínseca, es llamado shock obstructivo, ya que su causa es la obstrucción al flujo sanguíneo desde y hacia el corazón, aumentando la poscarga y disminuyendo la precarga cardíaca.
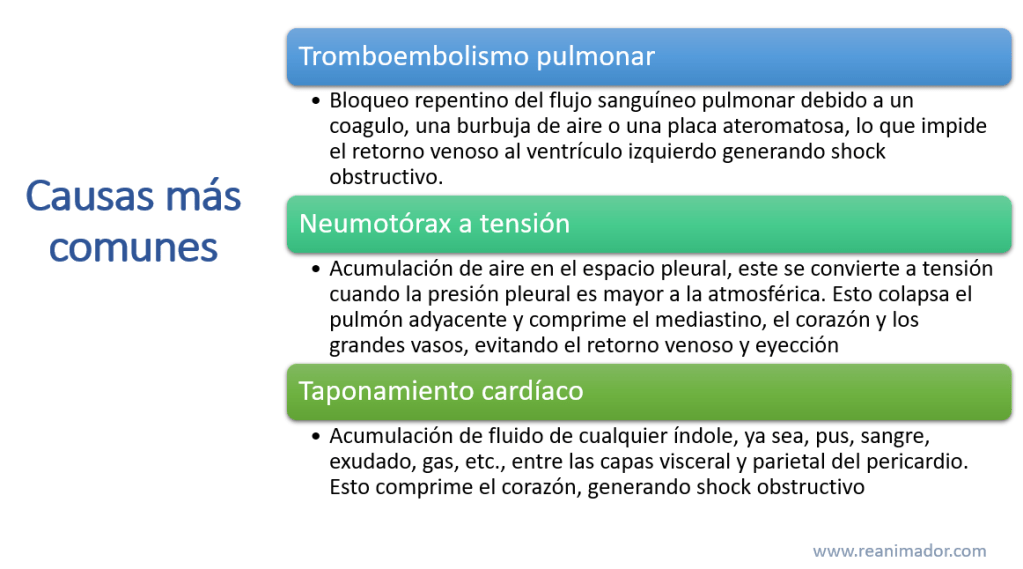
Existen tres grandes causas de shock obstructivo, la primera es la tromboembolia pulmonar, que consiste en un bloqueo repentino del flujo sanguíneo pulmonar debido a un coagulo, una burbuja de aire, o una placa ateromatosa, lo que impide el retorno venoso al ventrículo izquierdo. La segunda es el neumotórax a tensión, que es la acumulación de aire en el espacio pleural, este se convierte a tensión cuando la presión pleural es mayor a la atmosférica, lo que colapsa el pulmón adyacente y comprime el mediastino, el corazón y los grandes vasos, evitando el retorno venoso y la eyección sanguínea. La tercera causa es el taponamiento cardíaco, que consiste en la acumulación de fluido de cualquier índole, ya sea, pus, sangre, exudado o gas, entre las capas visceral y parietal del pericardio. Esto comprime el corazón y los grandes vasos evitando el retorno venoso, lo que, al igual que en el neumotórax a tensión, disminuye la precarga y aumenta la poscarga cardíaca.
La presentación clínica depende de la patología subyacente tras el shock obstructivo. En el caso de la tromboembolia pulmonar, el paciente presentará signos de insuficiencia cardiaca derecha. En el 80% de los caso se verá disneico, cerca del 70% presentará dolor torácico y taquipnea. Otros síntomas menos frecuentes son: tos, hemoptisis, taquicardia, trombosis venosa profunda, cianosis y síncope. Mientras más síntomas presente el paciente, más probabilidad que la tromboembolia pulmonar sea en un gran vaso, y por lo tanto, más riesgo de evolucionar a shock obstructivo. Cuando la patología que origina el shock es el taponamiento cardíaco, el paciente presentará pulso paradojal, que consiste en la desaparición del pulso durante la fase inspiratoria y su reaparición durante la fase espiratoria, sumado a triada de Beck, que consiste en ingurgitación yugular, ruidos cardíacos apagados e hipotensión arterial. La tercera patología, que comúnmente evoluciona a shock obstructivo es el neumotórax a tensión. La presentación clínica del neumotórax a tensión es, en un 96% de los casos, dolor torácico punzante, que se exacerba durante la inspiración. Otros signos clínicos que refuerzan el diagnóstico son: ventilación asimétrica, pulso paradojal, desviación traqueal y disminución o abolición del murmullo pulmonar en el hemitórax afectado.
Una herramienta útil para la sospecha diagnóstica de shock es el índice de shock, que se define como el cociente entre la frecuencia cardíaca y la presión arterial. Valores mayores a 0,9 en este índice reflejan un mal funcionamiento del ventrículo izquierdo, por lo que refuerzan el diagnóstico de shock de cualquier tipo.

1.2 Manejo prehospitalario del shock
El manejo prehospitalario del shock, al igual que en todas las patologías urgentes en el ámbito prehospitalario, debe guiarse por el análisis sistemático. En la letra X los reanimadores se centrarán en la compresión y contención de hemorragias exanguinantes, esto puede ser con apósitos normales o empapados en agentes hemostáticos o con torniquetes.
Cuando la vía aérea se encuentra comprometida los reanimadores deben permeabilizarla inicialmente, luego protegerla, y proveerla de oxígeno, para esto es necesario considerar el uso de pinzas de Maguill, cánula orofaríngea, máscara laríngea o intubación orotraqueal. Para proveer la vía aérea de oxígeno contará con distintos medios, como nariceras, mascarilla de Venturi o mascarilla con reservorio de no reinhalación. Finalmente puede apoyar la ventilación con una bolsa de reanimación, a través de una mascarilla, de un tubo orotraqueal o una máscara laríngea. Cuando el paciente se encuentra en shock obstructivo por un neumotórax a tensión los reanimadores deben drenar el aire pleural con una bránula, procedimiento llamado toracocentesis, en cambio, cuando es afectado por un taponamiento cardíaco, el drenaje debe ser pericárdico, a través de una pericardiocentesis, este procedimiento se realiza con una jeringa, como se detallará en la unidad de trauma torácico.
Para el manejo de las alteraciones de la circulación debemos comprimir las hemorragias no exanguinantes, con el fin de evitar pérdidas de volumen sanguíneo y reponer el volumen vascular perdido, para esto es necesario obtener al menos dos accesos vasculares de grueso calibre, con el objetivo de suministrar suero fisiológico, ojalá a 37 grados Celcius, hasta obtener una presión arterial sistólica sobre 90 o presión arterial media sobre 65 milímetros de mercurio. Si esto no da resultados positivos, se pueden usar fármacos vasopresores, los dos más ampliamente difundidos con este fin son, noradrenalina, cuya dosis varía entre 0,05 microgramos por kilo por minuto, y adrenalina, en dosis de 2 a 10 microgramos por kilo por minuto, el suministro de ambos fármacos debe ser a través de una bomba de infusión continua. En el manejo del shock anafiláctico prehospitalario se puede usar 0,5 miligramos de adrenalina vía intramuscular, hidrocortisona como agente corticoide antiinflamatorio y algún antihistamínico, como clorfenamina, para complementar la terapia general.

Una de las acciones cruciales en el manejo prehospitalario del shock es la protección de la vía aérea. El único dispositivo capaz de lograr ese fin en el medio prehospitalario es el tubo orotraqueal, lamentablemente, su instalación requiere de entrenamiento, ya que es una técnica compleja, por lo que no debe ser realizada de rutina. Existen una serie de indicaciones de intubación endotraqueal, estas son: disnea extrema, saturación de oxígeno inferior a 90%, a pesar de una fracción inspirada de oxígeno superior al 80%, obstrucción de la vía aérea superior refractaria a maniobras de desobstrucción, estatus convulsivo, quemaduras de la vía aérea, o incapacidad de mantener la vía aérea por fracturas faciales, o de protegerla por pérdida de reflejos protectores como el tusígeno o el nauseoso.
Para realizar una intubación orotraqueal, los reanimadores deben realizar una serie de pasos. El primero es la preparación del material y la evaluación del paciente. El material a utilizar será un tubo orotraqueal, una guía para el tubo, un laringoscopio, una bolsa de reanimación y un fijador de tubo. El segundo paso es la preoxigenación y estabilización, es altamente deseable que el paciente se encuentre con una presión arterial normal y una saturación parcial de oxígeno sobre el 90% previo a la laringoscopía. El tercer paso es la premedicación, con el fin de sedar y paralizar al paciente, para eso usaremos un fármaco sedante, de estar disponible, debe preferir el uso de fentanilo entre 2 a 3 microgramos por kilo. Como inductor del sueño se usará Etomidato en dosis de 0,3 miligramos por kilo, o Ketamina entre 1 y 2 milígramos por kilo de peso corporal, y como paralizante, los reanimadores usarán entre 1,5 y 2 milígramos por kilo de succinilcolina. Mientras los fármacos hacen efecto, debe pasar al paso número cuatro, que consiste en la alineación de la vía aérea del paciente, llevando la cabeza a posición de olfateo. Posteriormente, con el paciente en posición de olfateo, sedado y paralizado, se realizará la laringoscopía y la intubación, esto se logra pasando el tubo orotraqueal a través de las cuerdas vocales. Para finalmente realizar el paso 6, que consiste en probar la correcta instalación del tubo orotraqueal auscultando el epigastrio y ambos hemitórax, el resultado esperado de esta prueba es la ventilación simétrica bilateral sin ventilación en el epigastrio, para finalmente, fijar el tubo orotraqueal y conectar de un dispositivo de ventilación, que puede ser una bolsa de reanimación o un ventilador mecánico. Otra forma de probar la correcta instalación del tubo orotraqueal es obteniendo la concentración de dióxido de carbono al final de la espiración con un capnógrafo, cuando no hay capnografía registrable es altamente probable que el dispositivo se encuentre insertado en el esófago, lo que se puede reforzar con la auscultación epigástrica, si es así, debe ser retirado inmediatamente y realizar nuevamente todos los pasos, o en su defecto, insertar una máscara laríngea.
Preguntas
- ¿Cómo se define Shock?
- ¿Cuáles son los estadios de Shock?
- Explique el análisis sistemático de los pacientes en Shock
- ¿Qué tipos de Shock existen?
- ¿Qué es el Shock Hipovolémico?
- ¿Cuál es el manejo específico del Shock hipovolémico?
- ¿Qué es el Shock séptico?
- ¿Cuál es el manejo específico del Shock séptico?
- ¿Qué es el Shock anafiláctico y como se manifiesta?
- ¿Cuál es el manejo específico del Shock séptico?
- ¿Qué es el Shock neurogénico?
- ¿Cuál es el manejo específico del Shock neurogénico?
- ¿Qué es el shock cardiogénico?
- ¿Cuál es el manejo específico del Shock cardiogénico?
